Scientific journal
Научное обозрение. Педагогические науки
ISSN 2500-3402
ПИ №ФС77-57475
DEVELOPMENT OF AN OPTIMAL TECHNOLOGICAL LINE FOR THE PRODUCTION OF HYALURONIDASE USING MICROBIOLOGICAL SYNTHESIS
Ферменты в настоящее время применяются во многих областях, таких как медицина, пищевая промышленность, сельское хозяйство и других. В медицине ферменты получили очень широкое применение. Одной из групп ферментных препаратов являются препараты с действующим веществом гиалуронидазой [1].
Гиалуронидаза – фермент, который расщепляет основной компонент соединительной ткани – гиалуроновую кислоту [2]. Действие гиалуронидазы на гиалуроновую кислоту сводится к двум процессам: быстро протекающей деполимеризации и более медленному гидролизу, в результате которого в реакционной среде накапливаются N-ацетилглюкозамины и D-глюкуроновые кислоты [3].
Существует три типа гиалуронидаз, различающихся по механизму действия на гиалуроновые кислоты:
– Бактериальные гиалуронидазы;
– Гиалуронидазы из слюны пиявок;
– Тестикулярные гиалуронидазы [2].
Присутствующие на рынке, в данный момент, препараты с действующим веществом гиалуронидазой (лиаза, ронидаза и другие) производятся, в основном, с использованием тестикулярной гиалуронидазы, получаемой из семенников крупного рогатого скота. Однако, рациональной заменой такой гиалуронидазы может стать гиалуронидаза, произведённая с помощью микробиологического синтеза.
Целью данной работы является разработка технологической линии производства гиалуронидазы с использованием микробиологического синтеза.
Гиалуронидазы различного происхождения отличаются по своим физико-химическим и биологическим свойствам. Кроме того, даже гиалуронидазы одного вида, например, микробные гиалуронидазы, полученные из различных продуцентов, имеют существенные различия, хотя играют одну биологическую роль: в инфекционных процессах они отвечают за диссеминацию и проникновение болезнетворных бактерий в организмы животных и человека, то есть являются потенциальным вирулентным фактором.
Исследована способность 167 штаммов 15 видов спорообразующих аэробных бактерий из различных источников продуцировать свободную внеклеточную гиалуронидазу. 125 из 167 (75 %) исследованных источников характеризовались гиалуронидазной активностью. При сравнении физико-химических и биологических микробных гиалуронидаз, выявлены их существенные различия. Исследования гиалуронидазы из Staphylococcus aureus выявили наличие двух молекулярных форм гиалуронидазы с различной молекулярной массой. Оптимум действия этих двух форм наблюдается при рН = 5,0 – 7,2 и температуре от 30 до 37 °С. Фермент проявляет высокую специфичность к гиалуроновой кислоте и не действует на другие глюкозаминогликаны [3].
Таким образом, можно заключить, что микробная гиалуронидаза, в частности полученная из культуры Staphylococcus aureus, может применяться в терапевтических целях. Однако, для повышения безопасности производственного персонала, при получении данного препарата целесообразно использовать непатогенный штамм микроорганизмов, коим Staphylococcus aureus не является.
Для получения гиалуронидазы возможно использование штамма Pseudomonas putida. Этот штамм непатогенен и, кроме того, растёт на простых питательных средах и может синтезировать внеклеточные ферменты.
Известно, что Staphylococcus aureus продуцирует гиалуронидазу в количестве, необходимом для её производства. Таким образом, при сравнении продуктивности Pseudomonas putida со Staphylococcus aureus, можно сделать вывод о возможности использования Pseudomonas putida в качестве продуцента.
Из приведённых данных можно сделать вывод о том, что продуктивность штаммов Pseudomonas putida и Staphylococcus aureus отличается незначительно. Таким образом, использование Pseudomonas putida в качестве продуцента гиалуронидазы возможно. Кроме того, поскольку штамм Pseudomonas putida непатогенен, его использование безопасно, а значит – целесообразно. При глубинном способе культивирования, удельная активность гиалуронидазы выше, чем при поверхностном способе культивирования, к тому же из поверхностных культур труднее получать высокоочищенные препараты из-за большого количества балластных веществ [1].
Для подбора оптимального времени культивирования следует провести исследование процесса биосинтеза.
Сравнительный анализ активности гиалуронидазы при твёрдофазном и глубинном методах культивирования [4]
|
Продуцент |
Способ культивирования |
Часы ферментации |
||||||||
|
24 |
48 |
72 |
||||||||
|
Сб*, мг / мл |
А**, Ед / мл |
Ауд***, Ед / мл |
Сб, мг / мл |
А, Ед / мл |
Ауд, Ед / мл |
Сб, мг / мл |
А, Ед / мл |
Ауд , Ед / мл |
||
|
Pseudomonas putida |
Поверхностный |
10,8 |
55,0 |
5,0 |
6,2 |
30,0 |
4,8 |
3,8 |
19,0 |
5,0 |
|
Глубинный |
10,3 |
61,0 |
5,9 |
5,6 |
30,0 |
5,4 |
4,3 |
30,0 |
6,9 |
|
|
Staphylococcus aureus |
Поверхностный |
13,0 |
70,0 |
5,4 |
10,0 |
50,0 |
5,0 |
7,2 |
43,0 |
5,0 |
|
Глубинный |
14,0 |
80,0 |
5,7 |
12,6 |
68,0 |
5,4 |
10,2 |
46,0 |
4,5 |
|
Примечание. *Сб – концетрация общего белка; **А – ферментативная активность; ***Ауд – удельная ферментативная активность.
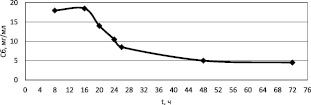
Изменения основных параметров при культивировании Pseudomonas putida с течением времени приведены на рис. 1 [4].
а)
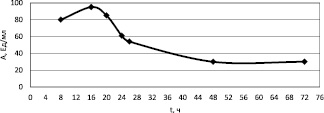
б)
Рис. 1. Изменение параметров в процессе ферментации (t): а – изменение концентрации общего белка (Сб ); б – гиалуронидазной активности (А)
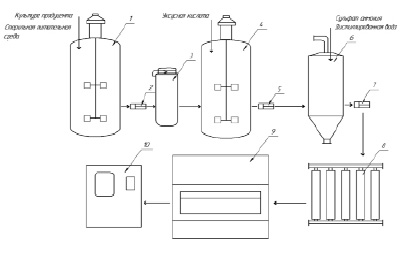
Рис. 2. Технологическая схема производства гиалуронидазы с использованием микробиологического синтеза. Условные обозначения: 1 – ферментёр; 2, 5, 7 – насосы; 3 – центрифуга; 4 – реактор для подкисления нативного раствора; 6 – сорбционная колонна; 8 – система ультрафильтрации; 9 – линия розлива; 10 – лиофильная сушилка
Из графиков, приведённых на рис. 2 видно:
– концентрация общего белка в нативном растворе возрастает до 16 часов ферментации, затем концентрация общего белка уменьшается;
– гиалуронидазная активность в первые часы ферментации возрастает, так как фермент является первичным метаболитом, и в начале ферментации активно растущие клетки выделяют его в культуральную жидкость. Максимум гиалуронидазной активности наблюдается в нативном растворе на 12 – 16 часов культивирования, затем активность гиалуронидазы уменьшается, так как фермент инактивируется с течением времени, особенно при повышенной температуре.
Таким образом, для получения гиалуронидазы целесообразно вести ферментацию до 16 часов, так как на этих часах культивирования в нативном растворе наблюдается максимальная активность фермента. Количественные характеристики нативного раствора Pseudomonas putida после 16 часов культивирования:
– концентрация общего белка – 17,7 мг/мл;
– концентрация углеводов – 1,7 мг/мл;
– гиалуронидазная активность – 96 Ед/мл;
– удельная гиалуронидазная активность – 5,4 Ед / мг белка;
– выход гиалуронидазы – 1920 Ед/г сухих клеток [4].
Для производства гиалуронидазы с использованием в качестве продуцента Pseudomonas putida была разработана технологическая схема, представленная на рис. 2.
Для производства гиалуронидазы по представленной выше технологической схеме в ферментёр 1 загружается стерильная питательная среда (состав: автолизат пивных дрожжей – 26,8 г/л; K2HPO4 – 1,5 г/л; MgSO4 – 1,5 г/л; вода), подогретая до 26–28 °С (pH 6,9 – 7,1), и суспензия клеток продуцента гиалуронидазы (Pseudomonas putida) плотностью от 5?105 до 106 клеток в 1 мл суспензии. Ферментация ведётся в течение 16 часов при температуре 26–30 °С, при pH 6,9–7,3. Во время ферментации постоянно ведётся контроль температуры и pH. После окончания ферментации культуральная жидкость, содержащая культуру продуцента, подаётся с помощью насоса 2 в центрифугу 3, где происходит отделение культуры продуцента от культуральной жидкости при вращении центрифуги со скоростью 6 000 – 6 500 об / мин. Полученный при центрифугировании нативный раствор поступает в реактор 4, где происходит его подкисление до значения pH 4,4–4,6 раствором уксусной кислоты (1 %) при постоянном перемешивании. Подкисленный нативный раствор подаётся насосом 5 в колонну с сорбентом 6, в которой белок, содержащий гиалуронидазу сорбируется на сульфокатионите КУ-23. После прохождения всего раствора через колонну, её промывают дистиллированной водой, после чего происходит десорбция белка раствором сульфата аммония при pH 9,1 – 9,4. Полученный элюат подаётся насосом 7 в систему ультрафильтрации 8, где происходит отделение белка от раствора солей и большей части воды. Белок, содержащий гиалуронидазу, поступает в систему розлива 9, в которой происходит розлив его во флаконы объёмом 10 мл. Флаконы укупориваются для лиофильной сушки и загружаются в полочную лиофильную сушилку 10. После сушки флаконы закрываются упаковываются. Характеристика готового продукта:
– Удельная гиалуронидазная активность – 58,9 ед / мг.
– pH-оптимум действия – 5,0.
– Температурный оптимум действия – 37 °С.
Произведённая методом микробиологического синтеза гиалуронидаза может применяться для лечения различных заболеваний, например, для профилактики и лечения артериальной гипертензии [5].
Выводы
Предложена технологическая линия производства препарата гиалуронидазы с целью лечения различных заболеваний на основе микробиологического синтеза с использованием непатогенного штамма микроорганизмов Pseudomonas putida.
Библиографическая ссылка
Чипинский Е.В. РАЗРАБОТКА ОПТИМАЛЬНОЙ ТЕХНОЛОГИЧЕСКОЙ ЛИНИИ ПРОИЗВОДСТВА ГИАЛУРОНИДАЗЫ С ИСПОЛЬЗОВАНИЕМ МИКРОБИОЛОГИЧЕСКОГО СИНТЕЗА // Научное обозрение. Педагогические науки. 2019. № 2-4. С. 106-109;URL: https://science-pedagogy.ru/en/article/view?id=2049 (дата обращения: 26.05.2026).


 science-review.ru
science-review.ru