Бадан толстолистый – многолетнее травянистое растение семейства каменоломковых. Укороченный надземный побег растения имеет на верхушке розетку, содержащую до двенадцати цельных, длинночерешковых, голых, кожистых листьев с закругленным основанием, длиной до 35 см и шириной до 30 см. Одно растение одновременно содержит зелёные, красные и чёрные листья. Зелёными листья остаются на протяжении двух-трёх лет, после чего краснеют. К концу четвёртого года листья чернеют [1].
Корневища и листья бадана содержат фенольные соединения, флавоноиды, каротиноиды, кумарины, арбутин, витамины, благодаря которым препараты из бадана проявляют противовоспалительное, антимикробное, противоопухолевое и адаптогенное действия. Широкий спектр воздействия обуславливает особый интерес к бадану в качестве перспективного растения для создания лекарственных препаратов с заданными фармакологическими свойствами, пищевых добавок и напитков [2-4]. В то же время для использования в медицинских целях в основном рассматриваются корневища растения, хотя содержание каротина, флавоноидов и аскорбиновой кислоты в листьях бадана значительно больше, чем в корневище [5]. Кроме того, химический состав исследуется, как правило, только на зелёных листьях бадана, тогда как содержание фармакологически активных соединений может быть не меньше в красных или чёрных листьях растения. В связи с чем целью данной работы являлось исследование содержания аскорбиновой кислоты (АК) в зелёных, красных и чёрных листьях бадана.
Основным методом количественного определения АК является титриметрический анализ с использованием 0,001 Н раствора 2,6-дихлофенолиндофенолята натрия (ГОСТ 3166-76). Однако этот метод имеет сложность с установлением конца титрования и практически не применим для окрашенных растительных вытяжек. Для многокомпонентных растительных проб также не применимо спектрофотометрическое определение АК, предполагающее расчёт её концентрации по коэффициенту молярной экстинции при 265 нм. Поэтому для анализа АК в растительных объектах активно применяются фотометрические методы, основанные на образовании интенсивно окрашенных соединений. Например, дегидроаскорбиновая кислота с 2,5-динитрофенилгидразином образует соединение, которое при взаимодействии с серной кислотой даёт осадок красного цвета [6].
В настоящей работе для количественного определения аскорбиновой кислоты в листьях бадана была применена спектрофотометрическая методика, основанная на цветной реакции аскорбиновой кислоты с фосфорно-молибденовым комплексом [7], которая показала свою эффективность на многих растительных объектах, в частности, при исследовании первоцвета весеннего [8].
Определение содержания аскорбиновой кислоты в анализируемых объектах данным методом может давать завышенные результаты по сравнению с хромотографическим определением, так как в реакцию окисления может вступать не только аскорбиновая кислота, но другие соединения, находящиеся в экстракте. Однако благодаря простоте выполнения, высокой чувствительности и экспрессности этот метод оптимален для проведения сравнительного определения содержания аскорбиновой кислоты в растительном материале.
Материалы и методы исследования
Объектами исследования являлись образцы высушенных зелёных, красных и чёрных листьев бадана, которые были заготовлены в 2017 г. в Кузбасском ботаническом саду Института экологии человека ФИЦ УУХ СО РАН г. Кемерово. Влажность сырья составляла не более 5 %. Имеющийся растительный материал перетирали в ступке до однородного порошкообразного состояния, гомогенизировали интенсивным встряхиванием в полимерных пакетах, после чего от образцов зелёных, красных и чёрных листьев отбирали по три точные навески. Отобранные навески заливали дистиллированной водой при соотношении сырье-экстрагент – 1:50 с добавлением 0,5 М раствора хлороводородной кислоты до достижения рН = 3,5. Выбор реакции среды для проведения экстракции АК связан с необходимостью её стабилизации в экстрактах. Известно, что по химической структуре АК является лактоном, содержащим две гидроксильные группы, которые проявляют слабые кислотные свойства (pK1 = 4,04; pK2 = 11,34). Поэтому можно считать, что при рН = 3,5 АК в растворе находится практически в недиссоциированной форме.
Экстракцию АК проводили при комнатной температуре в течение 30 мин при постоянном перемешивании смесей на шейкере. Полученные экстракты отфильтровывали через складчатые бумажные фильтры, после чего к 10 мл каждого фильтрата добавляли по 10 мл фосфорно-молибденового комплекса и выдерживали в течение суток. Поскольку АК является легкоокисляющимся соединением, то все операции по растиранию растительных образцов и фильтрованию экстрактов проводились при неярком искусственном освещении в максимально короткое время.
Оптическую плотность (D) полученных ярко-синих растворов определяли на фотометре КФК-3-01 при длине волны 730 нм в кварцевых кюветах с толщиной слоя 10 мм. В качестве растворов сравнения использовали соответствующие исходные экстракты. Расчёт содержания АК в пробах производили по калибровочной кривой, полученной по результатам измерения оптической плотности пяти модельных растворов стандартных образцов (РСО) аскорбиновой кислоты.
Приготовление модельных РСО АК
Для приготовления модельных растворов разной концентрации в мерные колбы вместимостью по 50 мл помещали рассчитанное количество АК (ФС 42-2668-95). Точные навески АК растворяли в 30 мл дистиллированной воды, добавляли 0,5 М раствор хлороводородной кислоты до рН = 3,5, после чего доводили объём растворов до метки и тщательно перемешивали. Хранение порошка АК осуществляли в холодильнике во флаконе из тёмного стекла.
Приготовление раствора фосфорно-молибенового комплекса
Навеску Na2HPO4?12H2O массой 0,050 г помещали в мерную колбу вместимостью 200 мл, растворяли в 90 мл дистиллированной воды, добавляли 10 мл концентрированной серной кислоты, прибавляли 50 мл дистиллированной воды и 0,80 г (NH4)2MoO4. После доведения объёма раствора до метки, смесь тщательно перемешивали.
Результаты исследования и их обсуждение
Калибровочный график D = f (С), полученный на модельных растворах РСО АК, характеризуется линейностью в диапазоне концентраций 5÷50 мкг/мл, и описывается коэффициентом детерминации r = 0,999906. Результаты определения концентрации АК в экстрактах листьев бадана разного цвета представлены в таблице.
Полученные значения концентраций АК не противоречат имеющимся литературным данным [4, 5, 9] и свидетельствуют о том, что содержание АК в красных листьях бадана больше, чем в зелёных, тогда как содержание АК в чёрных листьях меньше, чем в красных, но больше, чем в зелёных.
Содержание аскорбиновой кислоты в листьях бадана разного цвета
|
Цвет листьев |
Содержание, мг % на 100 г сухой массы |
|
Зелёные Красные Чёрные |
41,0 ± 4,3 58,5 ± 5,6 48,0 ± 5,0 |
Изменение концентрации АК в листьях бадана может быть объяснено естественным циклом развития растения. Известно, что активно АК участвует в фотосинтезе и дыхании растений [10]. Тогда увеличенное содержание АК в красных листьях бадана связано с замедлением процесса фотосинтеза, в то время как синтез АК происходит с большей скоростью. Уменьшение концентрации АК в чёрных листьях по отношению к концентрации в красных листьях определяется неизбежными процессами разложения вещества в неживых клетках.
Исследование кинетики окисления АК фосфорно-молибденовым комплексом
Интерес к изучению кинетики окисления АК в данной работе связан с необходимостью подтверждения факта полного завершения реакции её взаимодействия с фосфорно-молибденовым комплексом к моменту определения оптической плотности анализируемых растительных проб.
Изучение кинетики окисления АК проводилось с применением условия псевдопервого порядка, то есть реакцию образования молибденовой сини проводили при заведомом избытке фосфорно-молибденового комплекса.
Для снятия кинетических кривых были приготовлены модельные РСО АК разной концентрации. Изменение концентрации АК в реакции с фосфорно-молибденовым комплексом оценивали по величине оптической плотности, которую определяли на фотометре КФК-3-01 при длине волны 730 нм в кварцевых кюветах с толщиной слоя 10 мм. В качестве раствора сравнения использовали раствор фосфорно-молибденового комплекса соответствующей концентрации. Реакцию проводили непосредственно в кювете фотометра. Значения оптической плотности фиксировали с интервалом в 1 мин.
На основании проведённых экспериментов установлено, что применяемая в настоящей работе реакция окисления АК в исследуемом диапазоне концентраций описывается законом скорости первого порядка. Для подтверждения полученного результата был проверен инвариант. Для этого были сняты кинетические кривые двух реакционных смесей с разной концентрацией АК, при этом прямые, построенные в координатах ln C – t, являются параллельными (рисунок). Отклонения прямых от линейности не превышают погрешность эксперимента.
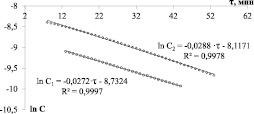
Зависимость lnС от времени при концентрациях АК: C1 = 0,072 ммоль/л, С2 = 0,114 ммоль/л
Таким образом, в границах анализируемой части кинетической кривой с получением линейной зависимости в координатах ln C – t был подтверждён первый порядок реакции окисления АК фосфорно-молибденовым комплексом, на что указывает неизменяемое значение коэффициента скорости реакции. Полученный результат свидетельствует о правомерности использования реакции окисления АК фосфорно-молибденовым комплексом для определения концентрации АК в исследуемом растительном материале и достоверности числового содержания АК в зелёных, красных и чёрных листьях бадана.
Выводы
Определена концентрация аскорбиновой кислоты в зелёных, красных и чёрных листьях бадана толстолистного фотометрическим методом с применением фосфорно-молибденового комплекса. Установлено, что содержание аскорбиновой кислоты в красных листьях больше, чем в зелёных, но содержание аскорбиновой кислоты в чёрных листьях меньше, чем в красных, но больше, чем в зелёных.
Библиографическая ссылка
Радждип С., Бхавана П., Храмченко В.Е. СОДЕРЖАНИЕ АСКОРБИНОВОЙ КИСЛОТЫ В ЗЕЛЁНЫХ, КРАСНЫХ И ЧЁРНЫХ ЛИСТЬЯХ БАДАНА ТОЛСТОЛИСТНОГО // Научное обозрение. Педагогические науки. – 2019. – № 4-4. – С. 86-89;URL: https://science-pedagogy.ru/ru/article/view?id=2150 (дата обращения: 20.04.2024).


 science-review.ru
science-review.ru